Autor : Aleksandra Kurowska
2022-10-20 19:41
Już jest nowe obwieszczenie refundacyjnej. Lista leków będzie obowiązywać od 1 listopada. Zawiera różne nowości - w tym m.in. dla pacjentów chorych na SM.
Nowa lista dostępna jest tutaj:
http://dziennikmz.mz.gov.pl/legalact/2022/111/
Na razie w samym pdf, bez tabeli zamieszczanych na stronie MZ.
Aktualizacja - tu wymieniamy szczegółowo wszystkie zmiany
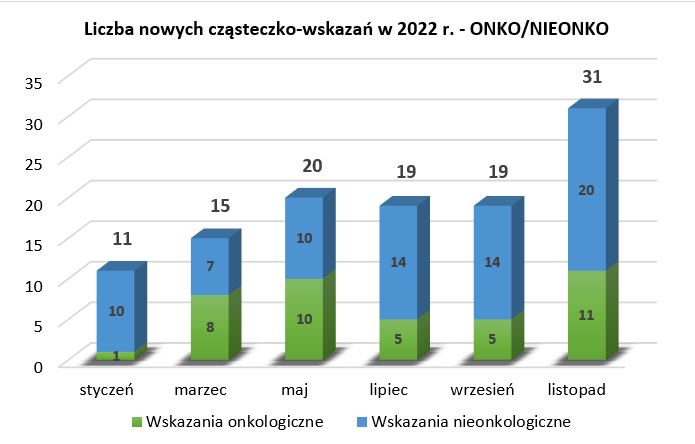 Refundacja: listopadowa lista z największą liczbą nowości
Refundacja: listopadowa lista z największą liczbą nowości
Analizę zmian opublikujemy po tym, jak MZ opublikuje dodatkowe dokumenty.
Przypomnijmy, że według projektu obwieszczenia w programach lekowych pojawi się 7 nowych substancji czynnych:
Glyceroli phenylbutyras – produkt Ravicti firmy Immedica Pharma AB (data wydania pierwszego pozwolenia na dopuszczenie do obrotu: 26 listopada 2015 r.) dostępny w ramach nowego programu lekowego B.140 Leczenie wspomagające zaburzeń cyklu mocznikowego (ICD-10: E72.2);
Inclisiranum – produkt Leqvio firmy Novartis Europharm Limited (data wydania pierwszego pozwolenia na dopuszczenie do obrotu: 9 grudnia 2020 r.) dostępny w ramach istniejącego programu lekowego B.101 Leczenie pacjentów z zaburzeniami lipidowymi (ICD-10: E78.01, I21, I22, I25);
Lutetium (177Lu) oxodotreotidi – produkt Lutathera firmy Advanced Accelerator Applications (data wydania pierwszego pozwolenia na dopuszczenie do obrotu: 26 września 2017 r.) dostępny w ramach nowego programu lekowego B.139 Leczenie pacjentów z nowotworami neuroendokrynnymi układu pokarmowego z zastosowaniem radiofarmaceutyków (ICD-10: C25.4, C17.0-C17.9, C18.0-C18.4);
Ofatumumabum – produkt Kesimpta firmy Novartis Ireland Limited (data wydania pierwszego pozwolenia na dopuszczenie do obrotu: 26 marca 2021 r.) dostępny w ramach istniejącego programu lekowego B.29 Leczenie chorych na stwardnienie rozsiane (ICD-10: G35);
Ozanimodum – produkt Zeposia firmy Bristol-Myers Squibb Pharma EEIG (data wydania pierwszego pozwolenia na dopuszczenie do obrotu: 20 maja 2020 r.) dostępny w ramach istniejącego programu lekowego B.29 Leczenie chorych na stwardnienie rozsiane (ICD-10: G35);
Ponesimodum – produkt Ponvory firmy Janssen-Cilag International N.V. (data wydania pierwszego pozwolenia na dopuszczenie do obrotu: 19 maja 2021 r.) dostępny w ramach istniejącego programu lekowego B.29 Leczenie chorych na stwardnienie rozsiane (ICD-10: G35);
Siponimodum – produkt Mayzent firmy Novartis Europharm Limited (data wydania pierwszego pozwolenia na dopuszczenie do obrotu: 13 stycznia 2020 r.) dostępny w ramach istniejącego programu lekowego B.29 Leczenie chorych na stwardnienie rozsiane (ICD-10: G35).
Zgodnie z projektem obwieszczenia w ramach programów lekowych wprowadzony zostanie pierwszy odpowiednik w ramach 1 substancji czynnej:
Abirateronum – z obniżką urzędowej ceny zbytu na poziomie od -66% do -68% w porównaniu do ceny jedynego dotychczas refundowanego leku z tą substancją czynną (produktu Zytiga firmy Janssen-Cilag International N.V.).
Projekt przewiduje także rozszerzenie zakresu finasowania o nowe programy lekowe dla 3 już refundowanych substancji czynnych:
Avelumabum – produkt Bavencio firmy Merck Europe B.V. włączony do nowego programu lekowego B.141 Leczenie pacjentów z rakiem urotelialnym (ICD-10: C61, C65, C66, C67, C68);
Baricitinibum – produkt Olumiant firmy Eli Lilly Nederland B.V. włączony do istniejącego programu lekowego B.124 Leczenie chorych z ciężką postacią atopowego zapalenia skóry (ICD-10: L20);
Upadacitinibum – produkt Rinvoq firmy AbbVie Deutschland GmbH & Co. KG włączony do istniejącego programu lekowego B.124 Leczenie chorych z ciężką postacią atopowego zapalenia skóry (ICD-10: L20).
Nowe leki refundowane będą też na rynku aptecznym.
Redaktor naczelna, od ponad 20 lat pracuje w mediach. Była redaktor naczelna Polityki Zdrowotnej, redaktor m.in. w Rzeczpospolitej, Dzienniku Gazecie Prawnej. Laureatka branżowych nagród dla dziennikarzy i mediów medycznych oraz Polskiej Izby Ubezpieczeń. Kontakt: aleksandra.kurowska@cowzdrowiu.pl